Какой объем раствора хлорида натрия с массовой долей соли 20%...
Задание:
Какой объем раствора хлорида натрия с массовой долей соли 20% и плотностью 1,15 г/мл надо прилить к 200 г воды, чтобы получить раствор с массовой долей соли 0,07?
Решение:
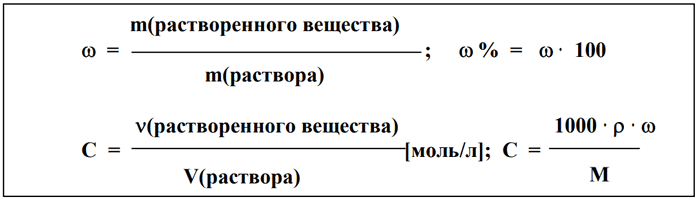
1) Обозначим массу исходного раствора за х, тогда масса хлорида натрия в нем будет равна:
m(NaCl) = m(исходного раствора) · ω(NaCl) = 0,2х.
2) Выражаем массу конечного раствора:
m(конечного раствора) = m(исходного раствора) + m(H2O) = х + 200.
3) Составляем уравнение и находим х:
m(NaCl) = m(конечного раствора) · ω(NaCl в конечном растворе); 0,2х = 0,07 · (х + 200);
0,2х = 0,07х + 14; 0,13х = 14; х = 107,7 г
4) Находим объем исходного раствора:
V(исходного раствора NaCl) = m(исходного раствора) / r(исходного раствора) = 107,7 / 1,15 = 93,7 мл.
Ответ: V(исходного раствора NaCl) = 93,7 мл