Определите массу осадка хлората калия(KClO3),выпавшего из раствора...
Задание:
Определите массу осадка хлората калия(KClO3),выпавшего из раствора, полученного смешиванием 100 г раствора хлората натрия (массовая доля соли 31,95 %) и 100 г раствора хлорида калия (массовая доля соли 22,35 %),если известно, что 33 коэффициент растворимости хлората калия в данных условиях равен 73 г на литр воды.
Решение:

1) Запишем уравнение реакции:

2) Определим массы и количества веществ в исходных растворах:
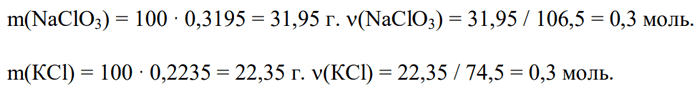
3) Определяем массу воды в исходных и конечном растворах:
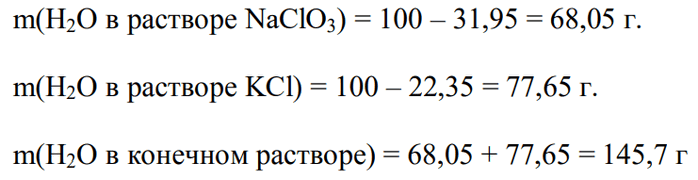
4) Определяем, какая масса KClO3 останется в конечном растворе, составляя следующую пропорцию:
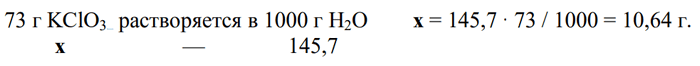
5) Рассчитываем массу осадка:
Всего согласно уравнению реакции может образоваться 0,3 моль KClO3, что соответствует массе = 0,3 · 122,5 = 36,75 г.
m(осадка) = 36,75 – 10,64 = 26,11 г.
Ответ: m(осадка) = 26,11 г.