Определите молекулярную формулу вещества, состоящего...
Задание:
Определите молекулярную формулу вещества, состоящего из кислорода, азота, фосфора и водорода, если известно, что оно содержит по массе 48,48 % кислорода, число атомов азота в нем в два раза больше числа атомов фосфора, а количество атомов водорода в соединении в 2,25 раза больше количества атомов кислорода. Молярная масса вещества меньше 200 г/моль.
Решение:

Формула вещества OxNyPzHk
1) Пусть масса вещества равна 100 г, тогда m(О) = 48,48 г. ν(О) = m(О) / М(О) = 48,48 / 16 = 3,03 моль.
2) ν(Н) = ν(О) · 2,25 = 3,03 · 2,25 = 6,82 моль. m(Н) = ν(Н) · М(Н) = 6,82 · 1 = 6,82 г
3) m(N + P) = m(вещества) - m(О) - m(Н) = 100 – 48,5 – 6,82 = 44,68 г.
m(N) = v(N) · M(N) = 14 ּ· v(N); m(P) = v(P) · M(P) = 31 · ν(P).
4) Составляем систему уравнений и решаем ее:
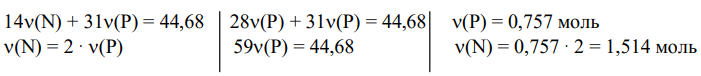
5) x : y : z : k = 3,03 : 1,514 : 0,757 : 6,82 = 4 : 2 : 1 : 9. O4N2PH9
Мы определили простейшую формулу вещества. Молекулярная формула может содержать удвоенное, утроенное и т.д. число атомов. Чтобы убедиться, что молекулярная формула совпадает с простейшей, подсчитаем молярную массу вещества:
М(O4N2PH9) = 16 · 4 + 14 · 2 + 31 + 1 · 9 = 132 г/моль. 132 < 200.
Очевидно, что молярная масса для удвоенной формулы будет больше 200, что противоречит условию задачи, следовательно, молекулярная формула вещества O4N2PH9. Перегруппировав атомы легко догадаться, что это вещество является гидрофосфатом аммония (NH4)2HPO4.
Ответ: (NH4)2HPO4.