Определите молярную концентрацию и массовую долю хлорида...
Категория: Химия | Добавлено: 01.05.2022
Задание:
Определите молярную концентрацию и массовую долю хлорида натрия в растворе, полученном растворением 14,63 г сухой соли в 100 мл воды (плотность раствора 1,146 г/мл).
Решение:
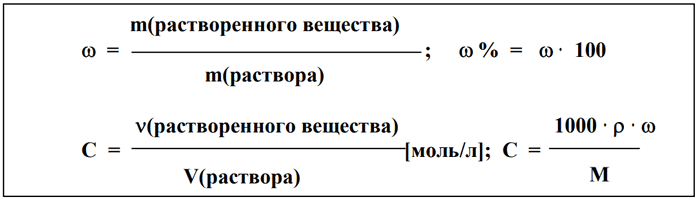
1) Находим массу раствора:
m(раствора) = m(растворенного вещества) + m(растворителя); m(Н2О) = V · ρ = 100 · 1 = 100 г
m(раствора) = m(NaCl) + m(H2O) = 14,63 + 100 = 114,63 г
2) ω(NaCl) = m(NaCl) / m(раствора) = 14,63 / 114,63 = 0,1276 (12,76 %)
3) Находим объем раствора, и количество вещества соли:
V(раствора) = m(раствора) / ρ(раствора) = 114,63 / 1,146 = 100 мл = 0,1 л.
v(NaCl) = m(NaCl) / M(NaCl) = 14,63 / 58,5 = 0,25 моль.
4) С(NaCl) = v(NaCl) / V(раствора) = 0,25 / 0,1 = 2,5 моль/л.
Ответ: ω(NaCl) = 12,76 %; С(NaCl) = 2,5 моль/л.