Определите молярные концентрации ионов в растворе сульфата...
Категория: Химия | Добавлено: 15.05.2022
Задание:
Определите молярные концентрации ионов в растворе сульфата алюминия с массовой долей соли 0,2 и плотностью 1,23 г/мл.
Решение:

1) Сульфат алюминия, как и подавляющее большинство солей, является сильным электролитом и диссоциирует в водном растворе полностью:
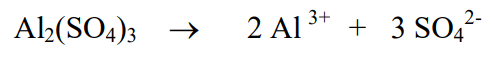
2) Пусть имеется 100 г раствора, тогда m(Al2(SO4)3) = 100 · 0,2 = 20 г, а V(раствора) = 100 / 1,23 = 81,3 мл = 0,0813 л.
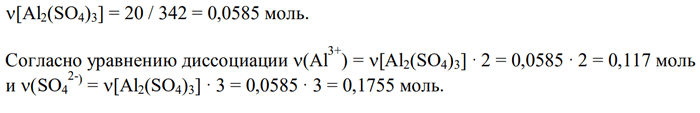
3) Вычисляем концентрации ионов в растворе:
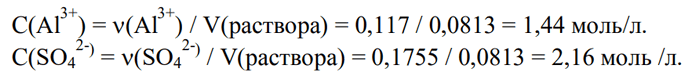
Ответ: С(Al3+) = 1,44 моль/л; С(SO42-) = 2,16 моль /л.